近日,大湾区大学(筹)理学院由才课题组与南方科技大学张绪穆、李秀秀团队合作,在三取代烯烃的不对称氢甲酰化反应中取得新进展。相关成果以 “Catalytic Regio- and Enantioselective Hydroformylation of Trisubstituted Alkenes to Construct α?Quaternary Lactams”为题发表在化学顶级期刊《美国化学会志》(J. Am. Chem. Soc.)上。由才助理教授在本研究中发挥了重要作用,杨玉红特任研究员为本论文的共同通讯作者,通过密度泛函理论(DFT)计算提供了关键的理论支持。大湾区大学(筹)理学院为论文的第二通讯单位。

研究背景
手性氮杂环化合物在药物研发、生物活性分子、天然产物及材料科学等领域备受关注,其中具有α-季碳中心的手性内酰胺因其显著的生物活性(如抗病毒潜力)及作为新型高分子结构单元的重要作用,成为研究热点。然而,传统合成方法在构建此类结构时面临反应条件苛刻、选择性控制困难等挑战。随着构效关系研究和新药开发对结构多样性需求的增加,开发兼容多底物、高效合成α-季碳β-和γ-内酰胺的新型催化体系已成为当前研究重点。
研究内容
本研究通过铑催化的三取代烯烃不对称氢甲酰化反应,实现了含α-季碳中心的β-和γ-内酰胺的高效构建。过渡金属催化的不对称氢甲酰化是一种原子经济性极高且环保的手性醛合成方法。然而,三取代烯烃的不对称氢甲酰化反应在构建季碳手性醛方面仍面临重大挑战:烯烃固有惰性、叔烷基金属铑中间体稳定性差、竞争性副反应(β-氢消除和氢化)以及取代基增多导致的选择性控制难题。通过优化催化体系,本研究成功克服了三取代烯烃的固有惰性以及Keulemans定律所限制的区域选择性挑战,使目标产物的区域选择性(rr)可达>20:1,非对映选择性(ee)高达99%。该方法在温和条件下进行,具有较高的原子经济性和良好的官能团兼容性,并适用于多种不同取代基的底物,展现了较好的合成普适性。此外,本研究还通过密度泛函理论(DFT)计算解析了反应的区域选择性和对映选择性的起源,揭示了铑-碳键结合模式及底物Boc基团与配体苯基之间的非共价相互作用对手性控制的关键作用。进一步的合成转化实验表明,该策略可用于合成多种具有潜在生物活性的手性内酰胺衍生物,为手性含氮杂环化合物的构建提供了一种高效且实用的催化体系。
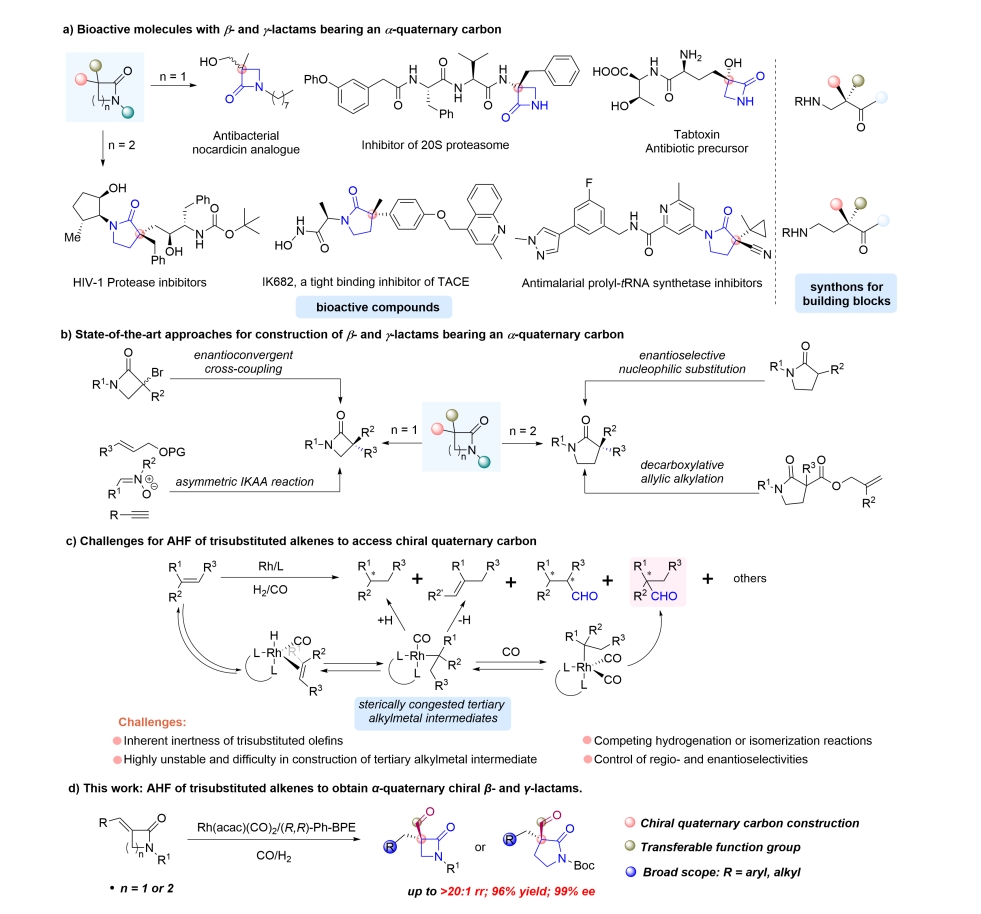
图1 研究背景和本文工作
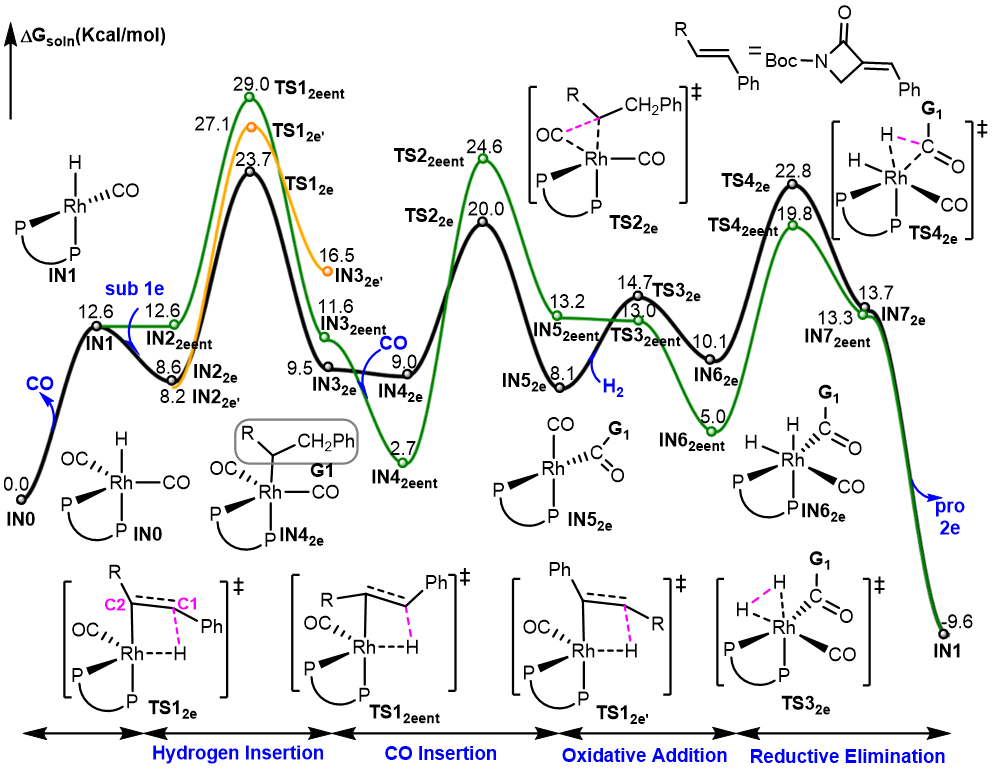
图2 DFT计算反应路径图